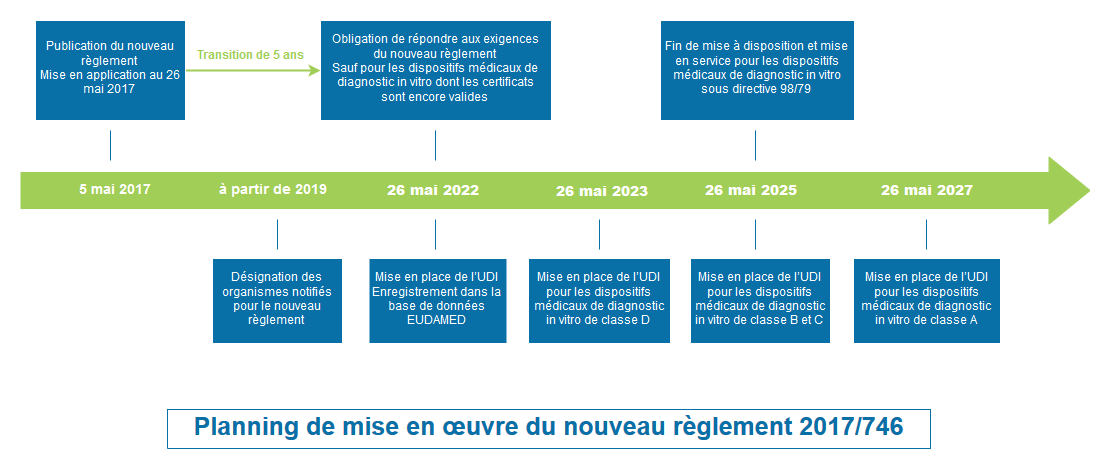
Entrée en vigueur et dates d’application (Article § 113)
- Publié au journal officiel de l’Union européenne le 5 avril 2017
- Entré en vigueur le 25 avril 2017
- Application obligatoire à partir du 26 mai 2022
Les certificats délivrés par des organismes notifiés (ou auto-déclarations) conformément à la directive 98/79/CE après le 25 avril 2017 conservent leur validité jusqu’à la fin de la période indiquée sur ces certificats, laquelle ne peut dépasser 5 ans. Ils sont toutefois invalidés au plus tard le 27 mai 2024.
Attention
- Les règles de classification des DMDIV changent sous le Règlement 2017/746. Un certain nombre de DMDIV marqués CE en auto-déclaration sous la Directive 98/79/CE devront faire l’objet d’une certification par un Organisme Notifié sous le Règlement 2017/746.
- Certaines dispositions sont applicables avant la date du 26 mai 2022, même pour les dispositifs marqués CE en autodéclaration sous la Directive 98/79/CE.
Les dates d’application en détail
Vous pourrez continuer à commercialiser vos dispositifs sous la Directive jusqu’à temps que vos certificats de conformité soient valides, même si cela intervient après la date d’application obligatoire du Règlement, le 26 mai 2022. Mais cette prolongation de mise sur le marché n’est possible que sous certaines conditions :
- Ne pas implémenter de changement significatif en ce qui concerne la conception du dispositif ou sa finalité
- Continuer à vous conformer aux exigences mentionnées par la Directive 98/79
Par contre, les dispositifs médicaux de diagnostic in vitro “autres” ne pourront plus être mis sur le marché en vertu de la Directive après le 26 mai 2022 : vos déclarations de conformité à la Directive ne feront plus foi passé cette date !
Il faudra donc effectuer la transition avant le 26 mai 2022 pour ce type de dispositifs.
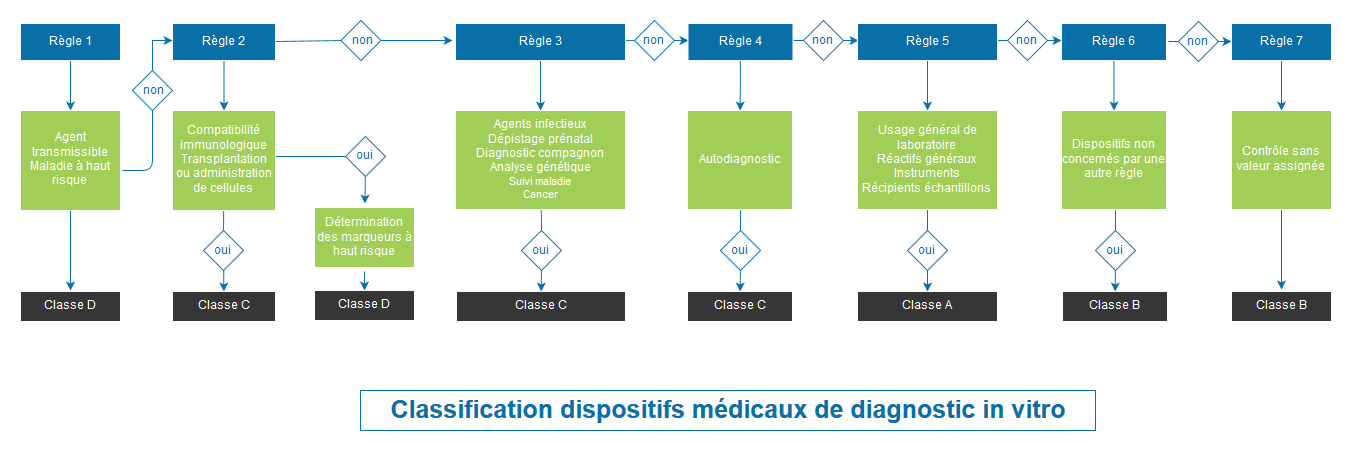
Classification des dispositifs médicaux selon le règlement 2017/746
Avec le règlement 2017/746, on assiste à une refonte complète du système de classification. La classification est basée sur le risque pour l’individu et la santé publique. Le Règlement prévoit 4 classes de dispositifs : A (classe la moins à risque), B, C et D (classe la plus à risque).
Les dispositifs des classes B, C et D, ainsi que les dispositifs de classe A stériles, seront soumis à l’évaluation d’un organisme notifié pour leur marquage CE.
C’est donc un évolution très importante et il est essentiel de déterminer la classe de vos dispositifs selon le Règlement 2017/746 le plus tôt possible afin d’anticiper les impacts au niveau de vos produits et de votre organisation.